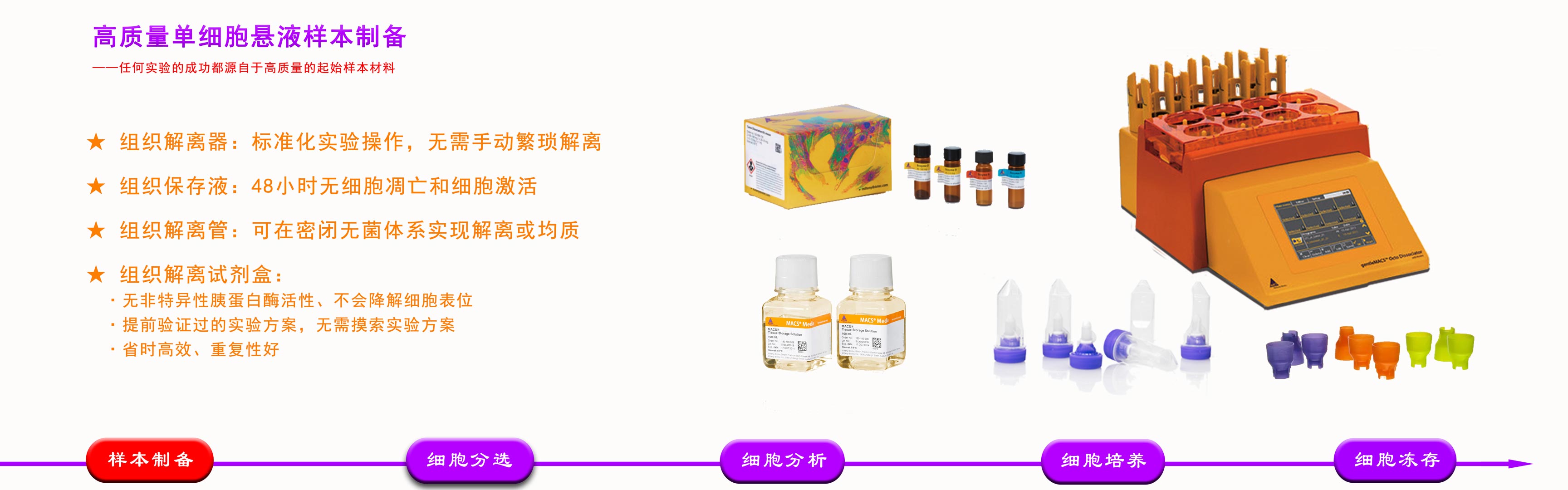
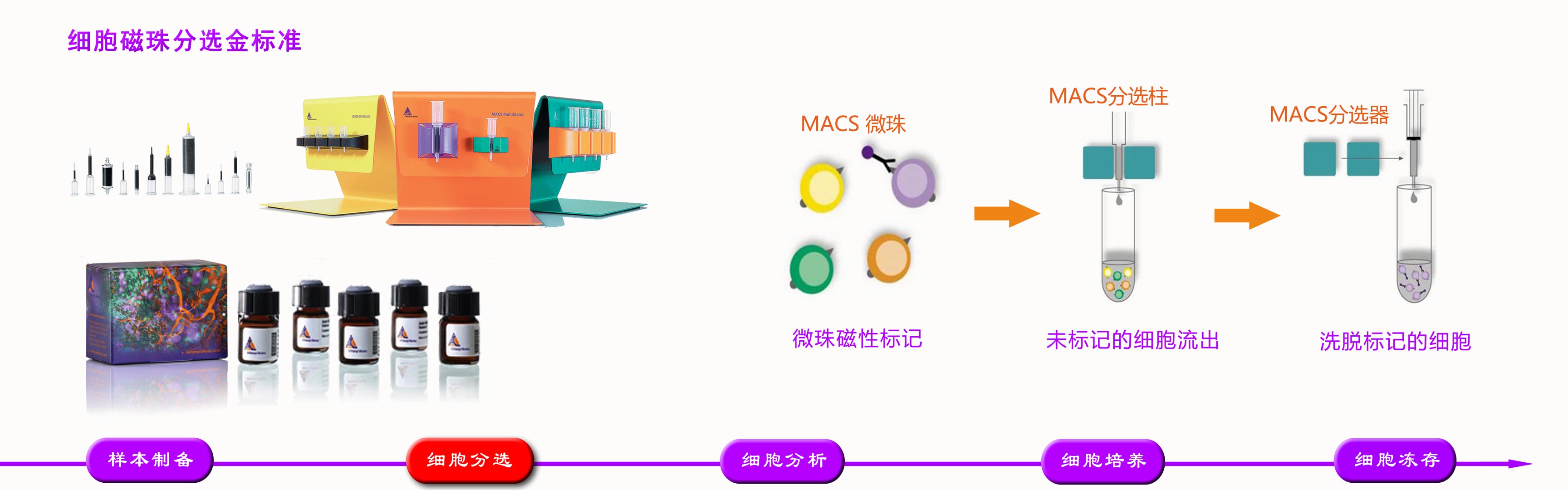
发布时间:2026-04-30
 抗体的选择
抗体的选择
●一抗选择:选择好用的一抗及其组合,TSA多色荧光标记成功了一半!那么我们该选择怎样的抗体呢 培镨生物跟您仔细讲讲
培镨生物跟您仔细讲讲
-
选择用于临床病理诊断的抗体。 -
选择文献报道的抗体。 -
尽量选择单抗,谨慎选择多抗。 -
小鼠标本不要选择小鼠来源的一抗(细胞染色除外)。 -
石蜡样本推荐Abcam标注IHC-P的抗体,尤以KO-VALIDATED (敲除验证)为佳。
●二抗选择:好的二抗也尤为重要
-
使用经过预吸附(也称交叉吸附)的二抗,以降低潜在物种交叉反应导致的非特异性背景,这对免疫细胞丰富的样本尤其重要。 -
尽量选择HRP直接标记的二抗:节省实验流程,提高特异性。 -
选择HRP多聚体二抗,可显著提高信噪比。 -
利用阳性样本进行抗体特异性验证:具有专业知识背景很重要!
-
查阅发表文献,获知抗原表达及抗体特异性的关键信息。 -
建议从DAB显色的IHC开始。 -
根据信号的组织定位、细胞定位、胞膜/胞核/胞浆/细胞器定位,综合验证抗体特异性。 -
记录获得最佳信号的一抗浓度、孵育时间和温度,二抗孵育时间,显色时间等关键信息。
![]() 荧光染料选择
荧光染料选择![]()
●TSA信号放大原理:了解背景知识,帮助我们得到更好的实验结果
1、TSA:HRP酶促反应在线性期内(0~T2)可持续活化1 0-1 000个荧光分子,反应最终饱和,进入平台期(T2-T3)。平台期之后,不同位点之间信号的差异会被逐渐拉平。
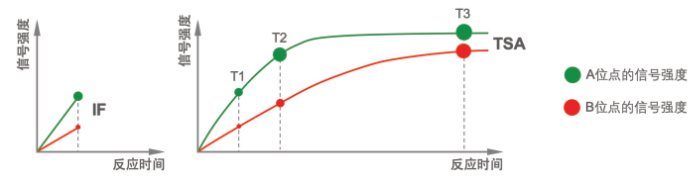
以CEP1 64的表达为例:CEP1 64在细胞中心体中高表达,在睫状囊泡中低表达,但在TSA标记过程中,过长反应时间(1 5 min)缩小了这种差异,让睫状囊泡中的信号看起来和中心体一样强。
由此可见,TSA对于低丰度靶点的检出具有巨大优势,但也要考虑信号放大过度造成的影响:
-
对于中高丰度靶点,请从原一抗浓度1 /1 0-1 /5开始测试使用TSA。
-
细胞实验请将TSA从1 :20~50稀释开始测试。
-
设置反应时间梯度,记录最佳反应时间。
-
如需考虑表达差异,应在T2之前中止反应。
2、TSA的占位效应
TSA荧光化合物在HRP催化下发生活化,与靶点附近的酪氨酸残基结合生成稳定的荧光化合物。
在多色标记过程中,当两个靶点抗原距离接近时,上一轮反应将抗原附近的酪氨酸耗竭,导致下一轮荧光结合不上的问题,称为占位效应。
-
TSA荧光化合物的作用半径为5~1 0nm,半径外的占位效应不会发生。
-
组织中的酪氨酸位点较为丰富,占位效应并不经常发生。
-
占位效应通常发生在距离接近且表达差异较大的靶点之间,例如PD1 和CD3,如果先做CD3并且信号放大过度,确实会导致PD1 染色弱甚至染不上的问题;某些表达广泛且丰度高的靶点,例如外源性表达的GFP分子,在信号放大过度时也可能会耗竭整个细胞的酪氨酸位点。
解决办法:“先低后高”、“先少后多”和适度原则:先染丰度低、表达范围少的靶点,后染丰度高、表达范围广的靶点。
关注培镨生物,了解更多相关知识